[1]
赵晨辰, 何向明, 王莉, 等.电化学还原CO2 阴极材料研究进展[J]. 化工进展, 2013, 32(2): 373⁃380.
[本文引用: 2]
[2]
Spinner N S, Vega J A, Mustain W E. Recent progress in the electrochemical conversion and utilization of CO2 [J]. Catalysis Science & Technology, 2012, 2(1): 19⁃28.
[本文引用: 1]
[3]
Sun Z Y, Ma T, Tao H C, et al. Fundamentals and challenges of electrochemical CO2 reduction using two⁃dimensional materials[J]. Chem, 2017, 3(4): 560⁃587.
[本文引用: 1]
[4]
Wang Y X, Niu C L, Wang D W. Metallic nanocatalysts for electrochemical CO2 reduction in aqueous solutions[J]. Journal of Colloid and Interface Science, 2018, 527: 95⁃106.
[本文引用: 1]
[5]
Schlögl R. Heterogeneous catalysis[J]. Angewandte Chemie International Edition, 2015, 54(11): 3465⁃3520.
[本文引用: 1]
[6]
张现萍, 黄海燕, 靳红利, 等.水溶液中电化学还原CO2 的研究进展[J]. 化工进展, 2015, 34(12): 4139⁃4144.
[本文引用: 1]
[7]
Yang W F, Dastafkan K, Jia C, et al. Design of electrocatalysts and electrochemical cells for carbon dioxide reduction reactions[J]. Advanced Materials Technologies, 2018, 3(9): 1700377.
[本文引用: 2]
[8]
Centi G, Quadrelli E A, Perathoner S. Catalysis for CO2 conversion: A key technology for rapid introduction of renewable energy in the value chain of chemical industries[J]. Energy & Environmental Science, 2013, 6(6): 1711⁃1731.
[本文引用: 1]
[9]
Kuhl K P, Cave E R, Abram D N, et al. New insights into the electrochemical reduction of carbon dioxide on metallic copper surfaces[J]. Energy & Environmental Science, 2012, 5(5): 7050⁃7059.
[本文引用: 2]
[10]
Hori Y, Murata A, Takahashi R. Formation of hydrocarbons in the electrochemical reduction of carbon dioxide at a copper electrode in aqueous solution[J]. Journal of the Chemical Society, Faraday Transactions 1: Physical Chemistry in Condensed Phases, 1989, 85(8): 2309⁃2326.
[本文引用: 1]
[11]
Mistry H, Varela A S, Bonifacio C S, et al. Highly selective plasma⁃activated copper catalysts for carbon dioxide reduction to ethylene[J]. Nature Communications, 2016, 7: 12123.
[本文引用: 3]
[12]
Rasul S, Anjum D H, Jedidi A, et al. A highly selective copper⁃indium bimetallic electrocatalyst for the electrochemical reduction of aqueous CO2 to CO[J]. Angewandte Chemie International Edition, 2015, 54(7): 2146⁃2150.
[本文引用: 2]
[13]
Raciti D, Livi K J, Wang C. Highly dense Cu nanowires for low⁃overpotential CO2 reduction[J]. Nano Letters, 2015, 15(10): 6829⁃6835.
[本文引用: 2]
[14]
Xie M S, Xia B Y, Li Y W, et al. Amino acid modified copper electrodes for the enhanced selective electroreduction of carbon dioxide towards hydrocarbons[J]. Energy & Environmental Science, 2016, 9(5): 1687⁃1695.
[本文引用: 2]
[15]
Chen C S, Handoko A D, Wan J H, et al. Stable and selective electrochemical reduction of carbon dioxide to ethylene on copper mesocrystals[J]. Catalysis Science & Technology, 2015, 5(1): 161⁃168.
[本文引用: 1]
[16]
Ma M, Djanashvili K, Smith W A. Controllable hydrocarbon formation from the electrochemical reduction of CO2 over Cu nanowire arrays[J]. Angewandte Chemie International Edition, 2016, 55(23): 6680⁃6684.
[本文引用: 1]
[17]
Tang W, Peterson A A, Varela A S, et al. The importance of surface morphology in controlling the selectivity of polycrystalline copper for CO2 electroreduction[J]. Physical Chemistry Chemical Physics, 2012, 14(1): 76⁃81.
[本文引用: 2]
[18]
Manthiram K, Beberwyck B J, Alivisatos A P. Enhanced electrochemical methanation of carbon dioxide with a dlispersible nanoscale copper catalyst[J]. Journal of the American Chemical Society, 2014, 136(38): 13319⁃13325.
[本文引用: 2]
[19]
Qiu Y L, Zhong H X, Zhang T T, et al. Copper electrode fabricated via pulse electrodeposition: Toward high methane selectivity and activity for CO2 electroreduction[J]. ACS Catalysis, 2017, 7(9): 6302⁃6310.
[本文引用: 2]
[20]
Reske R, Mistry H, Behafarid F, et al. Particle size effects in the catalytic electroreduction of CO2 on Cu nanoparticles[J]. Journal of the American Chemical Society, 2014, 136(19): 6978⁃6986.
[本文引用: 2]
[21]
Loiudice A, Lobaccaro P, Kamali E A, et al. Tailoring copper nanocrystals towards C2 products in electrochemical CO2 reduction[J]. Angewandte Chemie, 2016, 128(19): 5883⁃5886.
[本文引用: 2]
[22]
Roberts F S, Kuhl K P, Nilsson A. High selectivity for ethylene from carbon dioxide reduction over copper nanocube electrocatalysts[J]. Angewandte Chemie International Edition, 2015, 54(17): 5179⁃5182.
[本文引用: 1]
[23]
Choi C, Cheng T, Flores Espinosa M, et al. A highly active star decahedron Cu nanocatalyst for hydrocarbon production at low overpotentials[J]. Advanced Materials, 2019, 31(6): 1805405.
[本文引用: 1]
[24]
Reller C, Krause R, Volkova E, et al. Selective electroreduction of CO2 toward ethylene on nano dendritic copper catalysts at high current density[J]. Advanced Energy Materials, 2017, 7(12): 1602114.
[本文引用: 1]
[25]
Sen S, Liu D, Palmore G T R. Electrochemical reduction of CO2 at copper nanofoams[J]. ACS Catalysis, 2014, 4(9): 3091⁃3095.
[本文引用: 2]
[26]
Chung J, Won D H, Koh J, et al. Hierarchical Cu pillar electrodes for electrochemical CO2 reduction to formic acid with low overpotential[J]. Physical Chemistry Chemical Physics, 2016, 18(8): 6252⁃6258.
[本文引用: 2]
[27]
Kim D, Kley C S, Li Y, et al. Copper nanoparticle ensembles for selective electroreduction of CO2 to C2 -C3 products[J]. Proceedings of the National Academy of Sciences, 2017, 114(40): 10560⁃10565.
[本文引用: 1]
[28]
Lv J J, Jouny M, Luc W, et al. A highly porous copper electrocatalyst for carbon dioxide reduction[J]. Advanced Materials, 2018, 30(49): 1803111.
[本文引用: 1]
[29]
Weng Z, Jiang J B, Wu Y S, et al. Electrochemical CO2 reduction to hydrocarbons on a heterogeneous molecular Cu catalyst in aqueous solution[J]. Journal of the American Chemical Society, 2016, 138(26): 8076⁃8079.
[本文引用: 1]
[30]
Lysgaard S, Mýrdal J S G, Hansen H A, et al. A DFT⁃based genetic algorithm search for AuCu nanoalloy electrocatalysts for CO2 reduction[J]. Physical Chemistry Chemical Physics, 2015, 17(42): 28270⁃28276.
[本文引用: 1]
[31]
Zhu W J, Zhang L, Yang P P, et al. Morphological and compositional design of Pd⁃Cu bimetallic nanocatalysts with controllable product selectivity toward CO2 electroreduction[J]. Small, 2018, 14(7): 1703314.
[本文引用: 3]
[32]
Hoang T T H, Verma S, Ma S, et al. Nano porous copper⁃silver alloys by additive⁃controlled electrodeposition for the selective electroreduction of CO2 to ethylene and ethanol[J]. Journal of the American Chemical Society, 2018, 140(17): 5791⁃5797.
[本文引用: 3]
[33]
Ma S, Sadakiyo M, Heima M, et al. Electroreduction of carbon dioxide to hydrocarbons using bimetallic Cu⁃Pd catalysts with different mixing patterns[J]. Journal of the American Chemical Society, 2016, 139(1): 47⁃50.
[本文引用: 2]
[34]
Zhuang T T, Liang Z Q, Seifitokaldani A, et al. Steering post⁃C-C coupling selectivity enables high efficiency electroreduction of carbon dioxide to multi⁃carbon alcohols[J]. Nature Catalysis, 2018, 1(6): 421⁃428.
[本文引用: 1]
[35]
Chang Z Y, Huo S J, Zhang W, et al. The tunable and highly selective reduction products on Ag@Cu bimetallic catalysts toward CO2 electrochemical reduction reaction[J]. The Journal of Physical Chemistry C, 2017, 121(21): 11368⁃11379.
[本文引用: 2]
[36]
Ren D, Ang B S H, Yeo B S. Tuning the selectivity of carbon dioxide electroreduction toward ethanol onoxidederived Cux Zn catalysts[J]. ACS Catalysis, 2016, 6(12): 8239⁃8247.
[本文引用: 2]
[37]
Li Q, Fu J J, Zhu W L, et al. Tuning Sn⁃catalysis for electrochemical reduction of CO2 to CO via the core/shell Cu/SnO2 structure[J]. Journal of the American Chemical Society, 2017, 139(12): 4290⁃4293.
[本文引用: 1]
[38]
Hu H J, Wang Y T, Du N, et al. Thermal treatment induced Cu⁃Sn core/shell nanowire array catalysts for highly efficient CO2 electroreduction[J]. ChemElectroChem, 2018, 5(24): 3854⁃3858.
[本文引用: 1]
[39]
Hou Y H, Erni R, Widmer R, et al. Synthesis and characterization of degradation⁃resistant Cu@CuPd nanowire catalysts for the efficient production of formate and CO from CO2 [J]. ChemElectroChem, 2019, 6(12): 3189⁃3198.
[本文引用: 3]
[40]
Yang H, Hu Y W, Chen J J, et al. Intermediates adsorption engineering of CO2 electroreduction reaction in highly selective heterostructure Cu⁃based electrocatalysts for CO production[J]. Advanced Energy Materials, 2019, 9(27): 1901396.
[本文引用: 2]
[41]
Yin Z, Gao D F, Yao S Y, et al. Highly selective palladium⁃copper bimetallic electrocatalysts for the electrochemical reduction of CO2 to CO[J]. Nano Energy, 2016, 27: 35⁃43.
[本文引用: 1]
[42]
Dai C C, Sun L B, Song J J, et al. Selective electroreduction of carbon dioxide to formic acid on cobalt⁃decorated copper thin films[J]. Small Methods, 2019, 3(11): 1900362.
[本文引用: 1]
[43]
Le M, Ren M, Zhang Z, et al. Electrochemical reduction of CO2 to CH3 OH at copper oxide surfaces[J]. Journal of the Electrochemical Society, 2011, 158(5): 45⁃49.
[本文引用: 1]
[44]
Li C W, Ciston J, Kanan M W. Electroreduction of carbon monoxide to liquid fuel on oxide⁃derived nanocrystalline copper[J]. Nature, 2014, 508(7497): 504⁃507.
[本文引用: 1]
[45]
Gu Z X, Yang N, Han P, et al. Oxygen vacancy tuning toward efficient electrocatalytic CO2 reduction to C2 H4 [J]. Small Methods, 2019, 3(2): 1800449.
[本文引用: 2]
[46]
Zhu Q G, Sun X F, Yang D X, et al. Carbon dioxide electroreduction to C2 products over copper⁃cuprous oxide derived from electrosynthesized copper complex[J]. Nature Communications, 2019, 10(1): 3851.
[本文引用: 1]
[47]
Ren D, Deng Y, Handoko A D, et al. Selective electrochemical reduction of carbon dioxide to ethylene and ethanol on copper(I) oxide catalysts[J]. ACS Catalysis, 2015, 5(5): 2814⁃2821.
[本文引用: 1]
[48]
Sarfraz S, Garcia⁃Esparza A T, Jedidi A, et al. Cu⁃Sn bimetallic catalyst for selective aqueous electroreduction of CO2 to CO[J]. ACS Catalysis, 2016, 6(5): 2842⁃2851.
[本文引用: 1]
[49]
Kas R, Kortlever R, Milbrat A, et al. Electrochemical CO2 reduction on Cu2 O⁃derived copper nanoparticles: Controlling the catalytic selectivity of hydrocarbons[J]. Physical Chemistry Chemical Physics, 2014, 16(24): 12194⁃12201.
[本文引用: 1]
[50]
Wang S B, Wang X C. Multifunctional metal⁃organic frameworks for photocatalysis[J]. Small, 2015, 11(26): 3097⁃3112.
[本文引用: 1]
[51]
Qiu Y L, Zhong H X, Zhang T T, et al. Selective electrochemical reduction of carbon dioxide using Cu based metal organic framework for CO2 capture[J]. ACS Applied Materials & Interfaces, 2018, 10(3): 2480⁃2489.
[本文引用: 1]
[52]
Tan X Y, Yu C, Zhao C T, et al. Restructuring of Cu2 O to Cu2 O@Cu⁃metal–organic frameworks for selective electrochemical reduction of CO2 [J]. ACS Applied Materials & Interfaces, 2019, 11(10): 9904⁃9910.
[本文引用: 1]
[53]
Qiu Y L, Zhong H X, Xu W B, et al. Tuning the electrocatalytic properties of a Cu electrode with organic additives containing amine group for CO2 reduction[J]. Journal of Materials Chemistry A, 2019, 7(10): 5453⁃5462.
[本文引用: 1]
[54]
Liu H, Xiang K S, Liu Y C, et al. Polydopamine functionalized Cu nanowires for enhanced CO2 electroreduction towards methane[J]. ChemElectroChem, 2018, 5(24): 3991⁃3999.
[本文引用: 1]
2
... 随着能源不断消耗,大气中CO2 的排放量逐年递增,由此引发的环境问题已成为全球关注的热点.如何减少CO2 排放、有效转化和利用CO2 已引起各国政府的高度关注.CO2 的固定和转化是降低其含量的有效途径之一[1 ] .CO2 电化学还原(ERC)技术是在常温常压条件下,利用电能(尤其是可再生能源发电)将CO2 与水直接反应生成合成气、甲酸、碳氢化合物、醇类等高附加值的化学品或液态燃料的新技术,是一条实现可再生能源存储与CO2 转化利用相耦合的绿色途径,对人类的可持续发展具有重要意义[2 ] .ERC技术不需要制氢、加温和加压额外消耗的能量,且设备投资少,其潜在的经济效益和环境效益引起了研究者广泛关注. ...
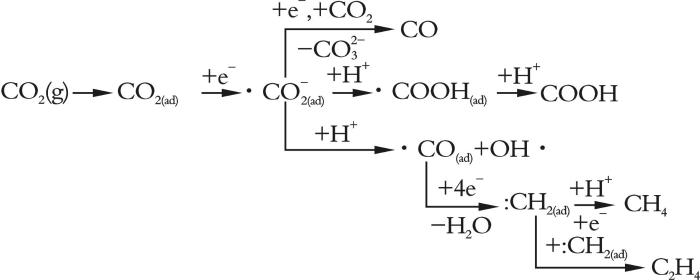
... (1)CO2 化学吸附在电催化剂上;(2)电子转移或质子迁移导致C-O的断裂或C-H的形成;(3)产物的结构重新排列以将其从电催化剂表面解吸并扩散到电解质中.被普遍接受的机理如图1 所示[1 ,6 ] . ...
1
... 随着能源不断消耗,大气中CO2 的排放量逐年递增,由此引发的环境问题已成为全球关注的热点.如何减少CO2 排放、有效转化和利用CO2 已引起各国政府的高度关注.CO2 的固定和转化是降低其含量的有效途径之一[1 ] .CO2 电化学还原(ERC)技术是在常温常压条件下,利用电能(尤其是可再生能源发电)将CO2 与水直接反应生成合成气、甲酸、碳氢化合物、醇类等高附加值的化学品或液态燃料的新技术,是一条实现可再生能源存储与CO2 转化利用相耦合的绿色途径,对人类的可持续发展具有重要意义[2 ] .ERC技术不需要制氢、加温和加压额外消耗的能量,且设备投资少,其潜在的经济效益和环境效益引起了研究者广泛关注. ...
1
... 近年来,ERC技术取得了长足进展,但仍存在许多亟待解决的问题,例如过电势高、缓慢的电子传递动力学、产物的选择性低、偏电流密度低、催化剂的稳定性与耐久性欠佳(小于100 h)等,上述问题限制了ERC技术的实际应用和商业化[3 ] .电催化剂作为ERC技术的关键材料,其性能直接影响CO2 转化效率、还原产物选择性及稳定性.因此,开发高性能的电催化剂,提高催化剂的催化活性、选择性和稳定性具有重要的研究意义和应用价值. ...
1
... ERC是一个多步骤反应过程,通常涉及多个电子反应途径[4 ] ,ERC多发生在电极⁃电解质界面,电催化剂作为工作电极,电解质有CO2 饱和水溶性、非水溶性电解液.在水溶性电解液中,ERC反应过程是一种非均相催化反应,涉及3个主要步骤[5 ] : ...
1
... ERC是一个多步骤反应过程,通常涉及多个电子反应途径[4 ] ,ERC多发生在电极⁃电解质界面,电催化剂作为工作电极,电解质有CO2 饱和水溶性、非水溶性电解液.在水溶性电解液中,ERC反应过程是一种非均相催化反应,涉及3个主要步骤[5 ] : ...
1
... (1)CO2 化学吸附在电催化剂上;(2)电子转移或质子迁移导致C-O的断裂或C-H的形成;(3)产物的结构重新排列以将其从电催化剂表面解吸并扩散到电解质中.被普遍接受的机理如图1 所示[1 ,6 ] . ...
2
... 在ERC反应过程中,施加的电极电位对最终还原产物有很大的影响.从热力学角度看,CO2 还原的平衡电位(相对于标准氢电极(SHE),在25 °C、101.325 kPa和1 mol/L的电解质水溶液中)与析氢反应的平衡电位相当,如反应式(1)-(8)所示[7 ] .H2 是水溶性电解液中CO2 电化学还原的主要副产物,如反应式(7)所示[7 ] ,因此将CO2 还原成具有良好选择性的理想产物具有很大挑战性. ...
... [7 ],因此将CO2 还原成具有良好选择性的理想产物具有很大挑战性. ...
1
... 在ERC反应中,电催化剂种类直接影响其催化活性和选择性[8 ] .在所有金属电催化剂中,Cu基催化剂是唯一可在水溶性电解质溶液中将CO2 高选择性地催化还原生成碳氢化合物和醇类的催化剂.在Cu基催化剂表面,CO2 可以还原成CO、HCOOH、CH4 、C2 H6 、C2 H4 及含氧碳氢化合物(醇类)等16种不同的还原产物[9 ] .不同的Cu基催化剂用于ERC反应时,还原产物分布不同.影响还原产物选择性和还原效率有多种因素,包括催化剂的结构、形貌、晶面、尺寸、组成、表面缺陷等.适宜的电催化剂应当具有足够有效的活性中心,能进一步提高CO2 的催化活性和产物的选择性,并可以减少耗能,同时具有较高的析氢过电位,能够有效抑制副反应的发生.但是,传统的金属Cu基催化剂存在催化活性低、过电位高及选择性差等问题.此外,长期电解还原过程中,Cu基催化剂的活性和选择性逐渐降低.Y.Hori等[10 ] 研究发现,Cu基催化剂表面覆盖的一层由石墨炭和Cu氧化物组成的黑色物质阻碍了CO2 与Cu基催化剂上的催化活性位接触,从而导致其几乎完全失活. ...
2
... 在ERC反应中,电催化剂种类直接影响其催化活性和选择性[8 ] .在所有金属电催化剂中,Cu基催化剂是唯一可在水溶性电解质溶液中将CO2 高选择性地催化还原生成碳氢化合物和醇类的催化剂.在Cu基催化剂表面,CO2 可以还原成CO、HCOOH、CH4 、C2 H6 、C2 H4 及含氧碳氢化合物(醇类)等16种不同的还原产物[9 ] .不同的Cu基催化剂用于ERC反应时,还原产物分布不同.影响还原产物选择性和还原效率有多种因素,包括催化剂的结构、形貌、晶面、尺寸、组成、表面缺陷等.适宜的电催化剂应当具有足够有效的活性中心,能进一步提高CO2 的催化活性和产物的选择性,并可以减少耗能,同时具有较高的析氢过电位,能够有效抑制副反应的发生.但是,传统的金属Cu基催化剂存在催化活性低、过电位高及选择性差等问题.此外,长期电解还原过程中,Cu基催化剂的活性和选择性逐渐降低.Y.Hori等[10 ] 研究发现,Cu基催化剂表面覆盖的一层由石墨炭和Cu氧化物组成的黑色物质阻碍了CO2 与Cu基催化剂上的催化活性位接触,从而导致其几乎完全失活. ...
... 单金属Cu基催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/V电解液 法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH 电抛光Cu箔 -1.05 0.1 mol/L KHCO3 40.6 [9 ] Cu纳米颗粒 -1.10 0.1 mol/L KClO4 1.0 36.0 37.0 <35.0 [17 ] n⁃Cu/C -1.35 0.1 mol/L NaHCO3 76.0 [18 ] Cu⁃P⁃ED -2.13 0.5 mol/L NaHCO3 85.0 [19 ] Cu箔 -1.10 0.1 mol/L KHCO3 57.0 20.0 <5.0 [20 ] 44 nm Cu纳米立方体 -1.10 0.1 mol/L KHCO3 41.0 46.4 [21 ] Cu纳米泡沫 -1.50(vs. ...
1
... 在ERC反应中,电催化剂种类直接影响其催化活性和选择性[8 ] .在所有金属电催化剂中,Cu基催化剂是唯一可在水溶性电解质溶液中将CO2 高选择性地催化还原生成碳氢化合物和醇类的催化剂.在Cu基催化剂表面,CO2 可以还原成CO、HCOOH、CH4 、C2 H6 、C2 H4 及含氧碳氢化合物(醇类)等16种不同的还原产物[9 ] .不同的Cu基催化剂用于ERC反应时,还原产物分布不同.影响还原产物选择性和还原效率有多种因素,包括催化剂的结构、形貌、晶面、尺寸、组成、表面缺陷等.适宜的电催化剂应当具有足够有效的活性中心,能进一步提高CO2 的催化活性和产物的选择性,并可以减少耗能,同时具有较高的析氢过电位,能够有效抑制副反应的发生.但是,传统的金属Cu基催化剂存在催化活性低、过电位高及选择性差等问题.此外,长期电解还原过程中,Cu基催化剂的活性和选择性逐渐降低.Y.Hori等[10 ] 研究发现,Cu基催化剂表面覆盖的一层由石墨炭和Cu氧化物组成的黑色物质阻碍了CO2 与Cu基催化剂上的催化活性位接触,从而导致其几乎完全失活. ...
3
... 近年来,研究者尝试使用氧化处理[11 ] 、合金化[12 ] 、形貌控制[13 ] 、表面改性[14 ] 等主要策略,精确调控催化剂的尺寸、组成、形貌和结构,提高Cu基催化剂的催化活性、选择性和稳定性.这些新型Cu基催化剂表现出催化活性高、对特定产物选择性高、过电位低等特点[15 ⁃16 ] .按照组成来分,可分为单金属Cu基催化剂、多金属Cu基催化剂及铜氧化物衍生催化剂等. ...
... C.W.Li等[44 ] 通过氧化退火处理Cu基催化剂,而后进行电化学还原表面的氧化层,发现表面修饰后的Cu电极比未修饰的Cu电极对ERC反应更有效,这可能与适当厚度的Cu2 O层电催化还原引起的晶界结构有关.H.Mistry等[11 ] 证明了氧化物衍生Cu基催化剂表面粗糙度对CO2 的催化性能有影响,Cu氧化物的存在是降低催化起始电位和提高催化活性的关键. ...
... Cu基催化剂的表面组成对ERC反应有重要影响.在Cu电极表面加入含氨基等官能团的有机物也可以有效调控Cu电极的性能.H.Mistry等[11 ] 对Cu电极表面进行氧等离子体改性,发现通过改性后的介孔泡沫Cu基催化剂对C2 烃类产物具有高的法拉第效率.M.S.Xie等[14 ] 通过氨基酸来修饰Cu纳米线,引入-NH3 + 2 和C3 等碳氢化合物.Y.L.Qiu等[53 ] 在Cu电极中添加含有-NH2 的甲酸甲酯(MC),利用MC中的-NH2 基团增加Cu电极表面活性位与ERC反应中间粒子(如COO*- 、CO*、CHO*等)结合强度,从而稳定中间粒子,增加对碳氢化合物的选择性,且降低电极表面的反应过电位,提高析氢过电位,抑制析氢副反应的发生.H.Liu等[54 ] 制备了一种新型的多巴胺包覆Cu纳米线(Cu NWs@PDA)催化剂,PDA上的氨基可以捕捉H+ ,使质子从电解质溶液中转移到催化界面,酚羟基可以调节Cu NWs与中间体CO*的稳定性,提升Cu NWs电极对CH4 的选择性和稳定性.Cu NWs和Cu NWs@PDA的还原产物CH4 的法拉第效率分别为13.0%和30.0%,Cu NWs@PDA在14 h内稳定性较好,有机物修饰后的Cu NWs提高了对CH4 的选择性. ...
2
... 近年来,研究者尝试使用氧化处理[11 ] 、合金化[12 ] 、形貌控制[13 ] 、表面改性[14 ] 等主要策略,精确调控催化剂的尺寸、组成、形貌和结构,提高Cu基催化剂的催化活性、选择性和稳定性.这些新型Cu基催化剂表现出催化活性高、对特定产物选择性高、过电位低等特点[15 ⁃16 ] .按照组成来分,可分为单金属Cu基催化剂、多金属Cu基催化剂及铜氧化物衍生催化剂等. ...
... 多金属Cu基催化剂也可以得到除了碳氢化合物之外的其他产物.S.Rasul等[12 ] 制备的Cu⁃In合金催化剂在0.1 mol/L KHCO3 电解液中高选择地生成CO,法拉第效率为80.0%.Q.Li等[37 ] 在Cu表面包覆一层薄薄的SnO2 氧化层(约0.8 nm)后,催化剂则对CO具有很高选择性(-0.70 V(vs. RHE),法拉第效率为93.0%).然而,当SnO2 氧化层的厚度增加到1.8 nm时,则对HCOOH的生成具有很高的活性和选择性.H.J.Hu等[38 ] 通过电化学与热处理结合的方式制备Cu⁃Sn核/壳纳米线阵列催化剂,在0.5 mol/L KHCO3 中总电流密度为-13.2~-19.3 mA/cm2 ,产物CO的法拉第效率基本保持在90.0%~91.4%.Y.H.Hou等[39 ] 制备出一种新型的Cu@CuPd纳米线催化剂,在0.5 mol/L KHCO3 电解液和-0.30 V(vs. RHE)电位下,HCOOH的法拉第效率可以达到80.0%,而在-0.80 V(vs. RHE)电位下,CO的法拉第效率长时间(20 h)不低于86.0%.H.Yang等[40 ] 采用煅烧和快速电偶置换法结合制备了异质结构纳米线(Cu2 O/CuO@M),Cu2 O/CuO@Ni纳米线具有较高的催化活性,在0.5 mol/L KHCO3 电解液和-1.20 V(vs. RHE)电位下,还原产物是CO的法拉第效率高达95.0%,Cu2 O/CuO纳米线与Ni纳米粒子的杂化不仅具有调节d带中心以提高本征活性的作用,还可以提高对COOH*中间体的吸附能力,抑制析氢反应,进一步提高电催化剂对CO的转化效率. ...
2
... 近年来,研究者尝试使用氧化处理[11 ] 、合金化[12 ] 、形貌控制[13 ] 、表面改性[14 ] 等主要策略,精确调控催化剂的尺寸、组成、形貌和结构,提高Cu基催化剂的催化活性、选择性和稳定性.这些新型Cu基催化剂表现出催化活性高、对特定产物选择性高、过电位低等特点[15 ⁃16 ] .按照组成来分,可分为单金属Cu基催化剂、多金属Cu基催化剂及铜氧化物衍生催化剂等. ...
... D.Raciti等[13 ] 制备的Cu纳米线在0.1 mol/L KHCO3 电解液中,-0.40 V(vs. RHE)电位下,CO产物的法拉第效率达到61.8%.在同种电解液中,S.Sen等[25 ] 采用粗糙的Cu纳米泡沫在-1.50 V(vs. SCE)电位下,还原产物为HCOOH的法拉第效率达到37.0%.J.Chung等[26 ] 报道的Cu纳米柱在-0.50 V(vs. RHE)电位下,将CO2 转化为HCOOH的法拉第效率为28.7%,而多孔的Cu纤维和Cu纳米线催化剂在低过电位下可以将CO2 高效转化为CO. ...
2
... 近年来,研究者尝试使用氧化处理[11 ] 、合金化[12 ] 、形貌控制[13 ] 、表面改性[14 ] 等主要策略,精确调控催化剂的尺寸、组成、形貌和结构,提高Cu基催化剂的催化活性、选择性和稳定性.这些新型Cu基催化剂表现出催化活性高、对特定产物选择性高、过电位低等特点[15 ⁃16 ] .按照组成来分,可分为单金属Cu基催化剂、多金属Cu基催化剂及铜氧化物衍生催化剂等. ...
... Cu基催化剂的表面组成对ERC反应有重要影响.在Cu电极表面加入含氨基等官能团的有机物也可以有效调控Cu电极的性能.H.Mistry等[11 ] 对Cu电极表面进行氧等离子体改性,发现通过改性后的介孔泡沫Cu基催化剂对C2 烃类产物具有高的法拉第效率.M.S.Xie等[14 ] 通过氨基酸来修饰Cu纳米线,引入-NH3 + 2 和C3 等碳氢化合物.Y.L.Qiu等[53 ] 在Cu电极中添加含有-NH2 的甲酸甲酯(MC),利用MC中的-NH2 基团增加Cu电极表面活性位与ERC反应中间粒子(如COO*- 、CO*、CHO*等)结合强度,从而稳定中间粒子,增加对碳氢化合物的选择性,且降低电极表面的反应过电位,提高析氢过电位,抑制析氢副反应的发生.H.Liu等[54 ] 制备了一种新型的多巴胺包覆Cu纳米线(Cu NWs@PDA)催化剂,PDA上的氨基可以捕捉H+ ,使质子从电解质溶液中转移到催化界面,酚羟基可以调节Cu NWs与中间体CO*的稳定性,提升Cu NWs电极对CH4 的选择性和稳定性.Cu NWs和Cu NWs@PDA的还原产物CH4 的法拉第效率分别为13.0%和30.0%,Cu NWs@PDA在14 h内稳定性较好,有机物修饰后的Cu NWs提高了对CH4 的选择性. ...
1
... 近年来,研究者尝试使用氧化处理[11 ] 、合金化[12 ] 、形貌控制[13 ] 、表面改性[14 ] 等主要策略,精确调控催化剂的尺寸、组成、形貌和结构,提高Cu基催化剂的催化活性、选择性和稳定性.这些新型Cu基催化剂表现出催化活性高、对特定产物选择性高、过电位低等特点[15 ⁃16 ] .按照组成来分,可分为单金属Cu基催化剂、多金属Cu基催化剂及铜氧化物衍生催化剂等. ...
1
... 近年来,研究者尝试使用氧化处理[11 ] 、合金化[12 ] 、形貌控制[13 ] 、表面改性[14 ] 等主要策略,精确调控催化剂的尺寸、组成、形貌和结构,提高Cu基催化剂的催化活性、选择性和稳定性.这些新型Cu基催化剂表现出催化活性高、对特定产物选择性高、过电位低等特点[15 ⁃16 ] .按照组成来分,可分为单金属Cu基催化剂、多金属Cu基催化剂及铜氧化物衍生催化剂等. ...
2
... 早期Cu基催化剂多以块体金属为主,一般常用多晶Cu箔或Cu板电极.近年来,研究者致力于开发不同形貌(纳米颗粒、纳米线、纳米棒、纳米花等)的Cu纳米电极,可以进一步改善其表面结构[17 ] ,以提高对目标产物的催化活性和选择性.表1 为单金属Cu基催化剂的CO2 还原产物比较结果. ...
... 单金属Cu基催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/V电解液 法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH 电抛光Cu箔 -1.05 0.1 mol/L KHCO3 40.6 [9 ] Cu纳米颗粒 -1.10 0.1 mol/L KClO4 1.0 36.0 37.0 <35.0 [17 ] n⁃Cu/C -1.35 0.1 mol/L NaHCO3 76.0 [18 ] Cu⁃P⁃ED -2.13 0.5 mol/L NaHCO3 85.0 [19 ] Cu箔 -1.10 0.1 mol/L KHCO3 57.0 20.0 <5.0 [20 ] 44 nm Cu纳米立方体 -1.10 0.1 mol/L KHCO3 41.0 46.4 [21 ] Cu纳米泡沫 -1.50(vs. ...
2
... 单金属Cu基催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/V电解液 法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH 电抛光Cu箔 -1.05 0.1 mol/L KHCO3 40.6 [9 ] Cu纳米颗粒 -1.10 0.1 mol/L KClO4 1.0 36.0 37.0 <35.0 [17 ] n⁃Cu/C -1.35 0.1 mol/L NaHCO3 76.0 [18 ] Cu⁃P⁃ED -2.13 0.5 mol/L NaHCO3 85.0 [19 ] Cu箔 -1.10 0.1 mol/L KHCO3 57.0 20.0 <5.0 [20 ] 44 nm Cu纳米立方体 -1.10 0.1 mol/L KHCO3 41.0 46.4 [21 ] Cu纳米泡沫 -1.50(vs. ...
... 在Cu基催化剂表面,CH4 是最易得到的还原产物,基本上各种结构的Cu基催化剂都可以得到CH4 .K.Manthiram等[18 ] 在玻碳上负载了Cu纳米粒子(n⁃Cu/C),其法拉第效率达到76.0%,与高纯Cu箔电极相比,电流密度大约是其4倍.Y.L.Qiu等[19 ] 采用脉冲电沉积法制备Cu电极,在-2.13 V(vs. RHE)电位下表现出较高的CH4 法拉第效率(85.0%),CH4 的电流密度可以达到-38 mA/cm2 ,高催化活性可能是由于电极具有较粗糙表面形貌,可以提供丰富的活性位点,使催化剂活性提高;增加的Cu(200)或Cu(100)面可能以台阶的形式引入到Cu(111)或Cu(110)晶面上,形成具有许多悬挂键的Cu(210)或Cu(533)晶面的台阶面,从而使其CH4 选择性大幅度提升. ...
2
... 单金属Cu基催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/V电解液 法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH 电抛光Cu箔 -1.05 0.1 mol/L KHCO3 40.6 [9 ] Cu纳米颗粒 -1.10 0.1 mol/L KClO4 1.0 36.0 37.0 <35.0 [17 ] n⁃Cu/C -1.35 0.1 mol/L NaHCO3 76.0 [18 ] Cu⁃P⁃ED -2.13 0.5 mol/L NaHCO3 85.0 [19 ] Cu箔 -1.10 0.1 mol/L KHCO3 57.0 20.0 <5.0 [20 ] 44 nm Cu纳米立方体 -1.10 0.1 mol/L KHCO3 41.0 46.4 [21 ] Cu纳米泡沫 -1.50(vs. ...
... 在Cu基催化剂表面,CH4 是最易得到的还原产物,基本上各种结构的Cu基催化剂都可以得到CH4 .K.Manthiram等[18 ] 在玻碳上负载了Cu纳米粒子(n⁃Cu/C),其法拉第效率达到76.0%,与高纯Cu箔电极相比,电流密度大约是其4倍.Y.L.Qiu等[19 ] 采用脉冲电沉积法制备Cu电极,在-2.13 V(vs. RHE)电位下表现出较高的CH4 法拉第效率(85.0%),CH4 的电流密度可以达到-38 mA/cm2 ,高催化活性可能是由于电极具有较粗糙表面形貌,可以提供丰富的活性位点,使催化剂活性提高;增加的Cu(200)或Cu(100)面可能以台阶的形式引入到Cu(111)或Cu(110)晶面上,形成具有许多悬挂键的Cu(210)或Cu(533)晶面的台阶面,从而使其CH4 选择性大幅度提升. ...
2
... 单金属Cu基催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/V电解液 法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH 电抛光Cu箔 -1.05 0.1 mol/L KHCO3 40.6 [9 ] Cu纳米颗粒 -1.10 0.1 mol/L KClO4 1.0 36.0 37.0 <35.0 [17 ] n⁃Cu/C -1.35 0.1 mol/L NaHCO3 76.0 [18 ] Cu⁃P⁃ED -2.13 0.5 mol/L NaHCO3 85.0 [19 ] Cu箔 -1.10 0.1 mol/L KHCO3 57.0 20.0 <5.0 [20 ] 44 nm Cu纳米立方体 -1.10 0.1 mol/L KHCO3 41.0 46.4 [21 ] Cu纳米泡沫 -1.50(vs. ...
... CO2 分子的化学惰性使其很难一步将其转化为C2+ 化合物,目前报道的Cu基催化剂对C2+ 产物的选择性和催化活性很低,且稳定性不满足要求.近几年,研究者通过调控催化剂的结构、形貌,使C2+ 产物的选择性明显提高.Cu基催化剂的尺寸效应对ERC反应的催化性能具有非常大的影响[20 ] .A.Loiudice等[21 ] 采用胶体化学法制备了3种不同粒径(24、44、63 nm)的Cu纳米立方体催化剂,粒径为44 nm的Cu纳米立方体的C2 H4 法拉第效率为41.0%(其中C2 H4 与CH4 的法拉第效率比为2.03),表现出最佳的催化活性,这可能是由于该催化剂的平面和边活性位之间达到最优的平衡,高密度的边缘原子促进C-C的偶联. ...
2
... 单金属Cu基催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/V电解液 法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH 电抛光Cu箔 -1.05 0.1 mol/L KHCO3 40.6 [9 ] Cu纳米颗粒 -1.10 0.1 mol/L KClO4 1.0 36.0 37.0 <35.0 [17 ] n⁃Cu/C -1.35 0.1 mol/L NaHCO3 76.0 [18 ] Cu⁃P⁃ED -2.13 0.5 mol/L NaHCO3 85.0 [19 ] Cu箔 -1.10 0.1 mol/L KHCO3 57.0 20.0 <5.0 [20 ] 44 nm Cu纳米立方体 -1.10 0.1 mol/L KHCO3 41.0 46.4 [21 ] Cu纳米泡沫 -1.50(vs. ...
... CO2 分子的化学惰性使其很难一步将其转化为C2+ 化合物,目前报道的Cu基催化剂对C2+ 产物的选择性和催化活性很低,且稳定性不满足要求.近几年,研究者通过调控催化剂的结构、形貌,使C2+ 产物的选择性明显提高.Cu基催化剂的尺寸效应对ERC反应的催化性能具有非常大的影响[20 ] .A.Loiudice等[21 ] 采用胶体化学法制备了3种不同粒径(24、44、63 nm)的Cu纳米立方体催化剂,粒径为44 nm的Cu纳米立方体的C2 H4 法拉第效率为41.0%(其中C2 H4 与CH4 的法拉第效率比为2.03),表现出最佳的催化活性,这可能是由于该催化剂的平面和边活性位之间达到最优的平衡,高密度的边缘原子促进C-C的偶联. ...
1
... F.S.Roberts等[22 ] 制备的Cu纳米管对C2 H4 具有较高的选择性.C.Choi等[23 ] 制备的星型十面体Cu纳米颗粒与商业化纳米相比,在-0.92~-0.98 V的C2 H4 法拉第效率升至50.7%.C.Reller等[24 ] 通过Br- 辅助生长树枝状Cu基催化剂,由于其具有高指数晶面和低配位数活性位,还原产物选择性生成C2 H4 法拉第效率达57.0%.以上结果表明,通过调控Cu基催化剂的组成和微观结构,构筑特殊形貌、活性位种类等方法可以提高催化剂的活性和对C2+ 产物选择性. ...
1
... F.S.Roberts等[22 ] 制备的Cu纳米管对C2 H4 具有较高的选择性.C.Choi等[23 ] 制备的星型十面体Cu纳米颗粒与商业化纳米相比,在-0.92~-0.98 V的C2 H4 法拉第效率升至50.7%.C.Reller等[24 ] 通过Br- 辅助生长树枝状Cu基催化剂,由于其具有高指数晶面和低配位数活性位,还原产物选择性生成C2 H4 法拉第效率达57.0%.以上结果表明,通过调控Cu基催化剂的组成和微观结构,构筑特殊形貌、活性位种类等方法可以提高催化剂的活性和对C2+ 产物选择性. ...
1
... F.S.Roberts等[22 ] 制备的Cu纳米管对C2 H4 具有较高的选择性.C.Choi等[23 ] 制备的星型十面体Cu纳米颗粒与商业化纳米相比,在-0.92~-0.98 V的C2 H4 法拉第效率升至50.7%.C.Reller等[24 ] 通过Br- 辅助生长树枝状Cu基催化剂,由于其具有高指数晶面和低配位数活性位,还原产物选择性生成C2 H4 法拉第效率达57.0%.以上结果表明,通过调控Cu基催化剂的组成和微观结构,构筑特殊形貌、活性位种类等方法可以提高催化剂的活性和对C2+ 产物选择性. ...
0.1 mol/L KHCO3 37.0 [25 ] Cu纳米柱 -0.50 0.1 mol/L KHCO3 28.7 [26 ] Cu纳米颗粒集合 -0.75 0.1 mol/L KHCO3 50.0 [27 ] 多孔纳米Cu -0.67 1.0 mol/L KOH 38.6 16.6 62.0 [28 ]
2.1.1 CH<sub>4</sub>产物 在Cu基催化剂表面,CH4 是最易得到的还原产物,基本上各种结构的Cu基催化剂都可以得到CH4 .K.Manthiram等[18 ] 在玻碳上负载了Cu纳米粒子(n⁃Cu/C),其法拉第效率达到76.0%,与高纯Cu箔电极相比,电流密度大约是其4倍.Y.L.Qiu等[19 ] 采用脉冲电沉积法制备Cu电极,在-2.13 V(vs. RHE)电位下表现出较高的CH4 法拉第效率(85.0%),CH4 的电流密度可以达到-38 mA/cm2 ,高催化活性可能是由于电极具有较粗糙表面形貌,可以提供丰富的活性位点,使催化剂活性提高;增加的Cu(200)或Cu(100)面可能以台阶的形式引入到Cu(111)或Cu(110)晶面上,形成具有许多悬挂键的Cu(210)或Cu(533)晶面的台阶面,从而使其CH4 选择性大幅度提升. ...
... D.Raciti等[13 ] 制备的Cu纳米线在0.1 mol/L KHCO3 电解液中,-0.40 V(vs. RHE)电位下,CO产物的法拉第效率达到61.8%.在同种电解液中,S.Sen等[25 ] 采用粗糙的Cu纳米泡沫在-1.50 V(vs. SCE)电位下,还原产物为HCOOH的法拉第效率达到37.0%.J.Chung等[26 ] 报道的Cu纳米柱在-0.50 V(vs. RHE)电位下,将CO2 转化为HCOOH的法拉第效率为28.7%,而多孔的Cu纤维和Cu纳米线催化剂在低过电位下可以将CO2 高效转化为CO. ...
0.1 mol/L KHCO3 37.0 [25 ] Cu纳米柱 -0.50 0.1 mol/L KHCO3 28.7 [26 ] Cu纳米颗粒集合 -0.75 0.1 mol/L KHCO3 50.0 [27 ] 多孔纳米Cu -0.67 1.0 mol/L KOH 38.6 16.6 62.0 [28 ]
2.1.1 CH<sub>4</sub>产物 在Cu基催化剂表面,CH4 是最易得到的还原产物,基本上各种结构的Cu基催化剂都可以得到CH4 .K.Manthiram等[18 ] 在玻碳上负载了Cu纳米粒子(n⁃Cu/C),其法拉第效率达到76.0%,与高纯Cu箔电极相比,电流密度大约是其4倍.Y.L.Qiu等[19 ] 采用脉冲电沉积法制备Cu电极,在-2.13 V(vs. RHE)电位下表现出较高的CH4 法拉第效率(85.0%),CH4 的电流密度可以达到-38 mA/cm2 ,高催化活性可能是由于电极具有较粗糙表面形貌,可以提供丰富的活性位点,使催化剂活性提高;增加的Cu(200)或Cu(100)面可能以台阶的形式引入到Cu(111)或Cu(110)晶面上,形成具有许多悬挂键的Cu(210)或Cu(533)晶面的台阶面,从而使其CH4 选择性大幅度提升. ...
... D.Raciti等[13 ] 制备的Cu纳米线在0.1 mol/L KHCO3 电解液中,-0.40 V(vs. RHE)电位下,CO产物的法拉第效率达到61.8%.在同种电解液中,S.Sen等[25 ] 采用粗糙的Cu纳米泡沫在-1.50 V(vs. SCE)电位下,还原产物为HCOOH的法拉第效率达到37.0%.J.Chung等[26 ] 报道的Cu纳米柱在-0.50 V(vs. RHE)电位下,将CO2 转化为HCOOH的法拉第效率为28.7%,而多孔的Cu纤维和Cu纳米线催化剂在低过电位下可以将CO2 高效转化为CO. ...
0.1 mol/L KHCO3 37.0 [25 ] Cu纳米柱 -0.50 0.1 mol/L KHCO3 28.7 [26 ] Cu纳米颗粒集合 -0.75 0.1 mol/L KHCO3 50.0 [27 ] 多孔纳米Cu -0.67 1.0 mol/L KOH 38.6 16.6 62.0 [28 ]
2.1.1 CH<sub>4</sub>产物 在Cu基催化剂表面,CH4 是最易得到的还原产物,基本上各种结构的Cu基催化剂都可以得到CH4 .K.Manthiram等[18 ] 在玻碳上负载了Cu纳米粒子(n⁃Cu/C),其法拉第效率达到76.0%,与高纯Cu箔电极相比,电流密度大约是其4倍.Y.L.Qiu等[19 ] 采用脉冲电沉积法制备Cu电极,在-2.13 V(vs. RHE)电位下表现出较高的CH4 法拉第效率(85.0%),CH4 的电流密度可以达到-38 mA/cm2 ,高催化活性可能是由于电极具有较粗糙表面形貌,可以提供丰富的活性位点,使催化剂活性提高;增加的Cu(200)或Cu(100)面可能以台阶的形式引入到Cu(111)或Cu(110)晶面上,形成具有许多悬挂键的Cu(210)或Cu(533)晶面的台阶面,从而使其CH4 选择性大幅度提升. ...
0.1 mol/L KHCO3 37.0 [25 ] Cu纳米柱 -0.50 0.1 mol/L KHCO3 28.7 [26 ] Cu纳米颗粒集合 -0.75 0.1 mol/L KHCO3 50.0 [27 ] 多孔纳米Cu -0.67 1.0 mol/L KOH 38.6 16.6 62.0 [28 ]
2.1.1 CH<sub>4</sub>产物 在Cu基催化剂表面,CH4 是最易得到的还原产物,基本上各种结构的Cu基催化剂都可以得到CH4 .K.Manthiram等[18 ] 在玻碳上负载了Cu纳米粒子(n⁃Cu/C),其法拉第效率达到76.0%,与高纯Cu箔电极相比,电流密度大约是其4倍.Y.L.Qiu等[19 ] 采用脉冲电沉积法制备Cu电极,在-2.13 V(vs. RHE)电位下表现出较高的CH4 法拉第效率(85.0%),CH4 的电流密度可以达到-38 mA/cm2 ,高催化活性可能是由于电极具有较粗糙表面形貌,可以提供丰富的活性位点,使催化剂活性提高;增加的Cu(200)或Cu(100)面可能以台阶的形式引入到Cu(111)或Cu(110)晶面上,形成具有许多悬挂键的Cu(210)或Cu(533)晶面的台阶面,从而使其CH4 选择性大幅度提升. ...
1
... 最近的研究表明,多金属复合是提高反应活性和选择性的有效方法之一,在Cu基催化剂中引入其他金属,可以调控催化剂的表面微观结构,从而调控其与反应中间体的结合能力,提高催化剂的电化学催化活性及还原产物的选择性.已报道的多金属纳米结构包括异质结构、合金结构和核壳结构等[29 ] .S.Lysgaard等[30 ] 发现Cu135 @Au174 核壳结构的纳米颗粒与Au309 具有相似的性质,说明核壳结构的催化剂可能具有壳的性能.合金结构的催化剂由于金属间的协同作用对特定产物的选择性有所提高.多金属铜基催化剂的CO2 还原产物比较结果见表2 . ...
1
... 最近的研究表明,多金属复合是提高反应活性和选择性的有效方法之一,在Cu基催化剂中引入其他金属,可以调控催化剂的表面微观结构,从而调控其与反应中间体的结合能力,提高催化剂的电化学催化活性及还原产物的选择性.已报道的多金属纳米结构包括异质结构、合金结构和核壳结构等[29 ] .S.Lysgaard等[30 ] 发现Cu135 @Au174 核壳结构的纳米颗粒与Au309 具有相似的性质,说明核壳结构的催化剂可能具有壳的性能.合金结构的催化剂由于金属间的协同作用对特定产物的选择性有所提高.多金属铜基催化剂的CO2 还原产物比较结果见表2 . ...
3
... 多金属铜基催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/V电解液 法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH CRD⁃Cu3 Pd -1.20 0.1 mol/L KHCO3 40.6 [31 ] FL⁃Pd3 Cu -0.90 0.1 mol/L KHCO3 82.1 [31 ] CuAg 纳米线 -0.70 1.0 mol/L KOH 60.0 25.0 85.0 [32 ] 相分离CuPd -0.74 1.0 mol/L KOH 48.0 15.0 63.0 [33 ] Ag@Cu⁃20 -1.06 0.1 mol/L KHCO3 28.6 [35 ] 氧化物衍生Cu4 Zn层 -1.05 0.1 mol/L KHCO3 0.4 10.8 29.1 10.4 0.3 [36 ] Cu@CuPd纳米线 -0.30 0.5 mol/L KHCO3 80.0 [39 ] Cu@CuPd纳米线 -0.80 0.5 mol/L KHCO3 86.0 [39 ] Cu2 O/CuO@Ni -1.20 0.5 mol/L KHCO3 95.0 [40 ] Pd85 Cu15 /C -0.89 0.1 mol/L KHCO3 86.0 [41 ] Cu/Co纳米线 -0.65 0.1 mol/L KHCO3 80.0 [42 ]
2.2.1 碳氢化合物 W.J.Zhu等[31 ] 制备的凹菱形十二面体Cu3 Pd(CRD⁃Cu3 Pd)催化剂催化ERC反应的初始电位较纯Cu箔降低了200 mV,在-1.20 V(vs. RHE)电位下,生成CH4 的法拉第效率最高为40.6%,是纯Cu箔的2倍,其高选择性源于低配位指数和组成效应的协同作用. ...
... [31 ]
CuAg 纳米线 -0.70 1.0 mol/L KOH 60.0 25.0 85.0 [32 ] 相分离CuPd -0.74 1.0 mol/L KOH 48.0 15.0 63.0 [33 ] Ag@Cu⁃20 -1.06 0.1 mol/L KHCO3 28.6 [35 ] 氧化物衍生Cu4 Zn层 -1.05 0.1 mol/L KHCO3 0.4 10.8 29.1 10.4 0.3 [36 ] Cu@CuPd纳米线 -0.30 0.5 mol/L KHCO3 80.0 [39 ] Cu@CuPd纳米线 -0.80 0.5 mol/L KHCO3 86.0 [39 ] Cu2 O/CuO@Ni -1.20 0.5 mol/L KHCO3 95.0 [40 ] Pd85 Cu15 /C -0.89 0.1 mol/L KHCO3 86.0 [41 ] Cu/Co纳米线 -0.65 0.1 mol/L KHCO3 80.0 [42 ]
2.2.1 碳氢化合物 W.J.Zhu等[31 ] 制备的凹菱形十二面体Cu3 Pd(CRD⁃Cu3 Pd)催化剂催化ERC反应的初始电位较纯Cu箔降低了200 mV,在-1.20 V(vs. RHE)电位下,生成CH4 的法拉第效率最高为40.6%,是纯Cu箔的2倍,其高选择性源于低配位指数和组成效应的协同作用. ...
... W.J.Zhu等[31 ] 制备的凹菱形十二面体Cu3 Pd(CRD⁃Cu3 Pd)催化剂催化ERC反应的初始电位较纯Cu箔降低了200 mV,在-1.20 V(vs. RHE)电位下,生成CH4 的法拉第效率最高为40.6%,是纯Cu箔的2倍,其高选择性源于低配位指数和组成效应的协同作用. ...
3
... 多金属铜基催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/V电解液 法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH CRD⁃Cu3 Pd -1.20 0.1 mol/L KHCO3 40.6 [31 ] FL⁃Pd3 Cu -0.90 0.1 mol/L KHCO3 82.1 [31 ] CuAg 纳米线 -0.70 1.0 mol/L KOH 60.0 25.0 85.0 [32 ] 相分离CuPd -0.74 1.0 mol/L KOH 48.0 15.0 63.0 [33 ] Ag@Cu⁃20 -1.06 0.1 mol/L KHCO3 28.6 [35 ] 氧化物衍生Cu4 Zn层 -1.05 0.1 mol/L KHCO3 0.4 10.8 29.1 10.4 0.3 [36 ] Cu@CuPd纳米线 -0.30 0.5 mol/L KHCO3 80.0 [39 ] Cu@CuPd纳米线 -0.80 0.5 mol/L KHCO3 86.0 [39 ] Cu2 O/CuO@Ni -1.20 0.5 mol/L KHCO3 95.0 [40 ] Pd85 Cu15 /C -0.89 0.1 mol/L KHCO3 86.0 [41 ] Cu/Co纳米线 -0.65 0.1 mol/L KHCO3 80.0 [42 ]
2.2.1 碳氢化合物 W.J.Zhu等[31 ] 制备的凹菱形十二面体Cu3 Pd(CRD⁃Cu3 Pd)催化剂催化ERC反应的初始电位较纯Cu箔降低了200 mV,在-1.20 V(vs. RHE)电位下,生成CH4 的法拉第效率最高为40.6%,是纯Cu箔的2倍,其高选择性源于低配位指数和组成效应的协同作用. ...
... T.T.H.Hoang等[32 ] 采用电沉积法制备了不同组分的CuAg纳米线,通过添加剂3,5⁃二氨基⁃1,2,4⁃三唑(DAT)来调控催化剂形貌,多孔纳米CuAg线在-0.70 V(vs.RHE)电位下,对C2+ 产物表现出较高的选择性,法拉第效率为85.0%.S.Ma等[33 ] 通过改变不同Cu、Pd原子配比及排列方式,制备出3种不同Cu⁃Pd合金催化剂,还原产物C2 H4 的选择性较高,相分离Cu⁃Pd催化剂法拉第效率可达48.0%.T.T.Zhuang等[34 ] 合成了缺陷可控的新型核⁃壳⁃空位铜(Cu2 S⁃Cu⁃V)纳米催化剂,通过催化剂核中掺杂硫原子并在壳层中引入铜空位,显著增强了多碳醇产物的选择性.Z.Y.Chang等[35 ] 采用一步还原法制备了不同Ag核、Cu修饰Ag核、Ag@Cu⁃20核壳结构纳米粒子催化剂,产物逐渐显示出由CO到碳氢化合物的变化,还原产物C2 H4 的法拉第效率为28.6%.D.Ren等[36 ] 制备了氧化物衍生的铜锌催化剂用于还原成乙醇,通过锌的质量控制乙醇的选择性,在-1.05 V(vs. RHE)条件下,Cu4 Zn对乙醇的选择性最好,达到29.1%,并5 h内保持稳定. ...
... Cu基催化剂的表面缺陷可以修饰和提高表面活性,因此被广泛用于电催化剂中.表面缺陷可以改变表面和次表面原子的配位环境,导致表面附近的电荷不平衡而增强电子的转移,进一步有效调节表面物种对催化剂的吸附[32 ] .郑耿锋课题组报道了一种含有氧空位的Cu基催化剂,在ERC反应中表现出较高的催化活性[45 ] .利用氧空位给CO2 提供大量的电子,有利于*CO、*COH中间产物的吸附及*CH2 的脱附,提高Cu基催化剂对C2 H4 的选择性,-1.40 V(vs. RHE)电位下,法拉第效率达到63.0%,且电流密度增大.氧空位的多少对C2 H4 产物有直接的影响,也会影响电流大小.韩布兴院士课题组通过原位电沉积Cu络合物的方法制备出三维树枝状Cu⁃Cu2 O复合材料[46 ] .在KCl为电解质溶液,-0.40 V(vs. RHE)电位下,过电位分别为0.53 V(CH3 COOH)和0.48 V(C2 H5 OH),C2+ 产物法拉第效率高达80.0%,电流密度为-11.5 mA/cm2 .其优异C2+ 产物选择性主要是由于电催化剂与Cu基底的接触电阻接近于0,同时在三维树突状结构中暴露出了丰富的活性位点,并具有合适的Cu(I)/Cu(0)活性位点比例. ...
2
... 多金属铜基催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/V电解液 法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH CRD⁃Cu3 Pd -1.20 0.1 mol/L KHCO3 40.6 [31 ] FL⁃Pd3 Cu -0.90 0.1 mol/L KHCO3 82.1 [31 ] CuAg 纳米线 -0.70 1.0 mol/L KOH 60.0 25.0 85.0 [32 ] 相分离CuPd -0.74 1.0 mol/L KOH 48.0 15.0 63.0 [33 ] Ag@Cu⁃20 -1.06 0.1 mol/L KHCO3 28.6 [35 ] 氧化物衍生Cu4 Zn层 -1.05 0.1 mol/L KHCO3 0.4 10.8 29.1 10.4 0.3 [36 ] Cu@CuPd纳米线 -0.30 0.5 mol/L KHCO3 80.0 [39 ] Cu@CuPd纳米线 -0.80 0.5 mol/L KHCO3 86.0 [39 ] Cu2 O/CuO@Ni -1.20 0.5 mol/L KHCO3 95.0 [40 ] Pd85 Cu15 /C -0.89 0.1 mol/L KHCO3 86.0 [41 ] Cu/Co纳米线 -0.65 0.1 mol/L KHCO3 80.0 [42 ]
2.2.1 碳氢化合物 W.J.Zhu等[31 ] 制备的凹菱形十二面体Cu3 Pd(CRD⁃Cu3 Pd)催化剂催化ERC反应的初始电位较纯Cu箔降低了200 mV,在-1.20 V(vs. RHE)电位下,生成CH4 的法拉第效率最高为40.6%,是纯Cu箔的2倍,其高选择性源于低配位指数和组成效应的协同作用. ...
... T.T.H.Hoang等[32 ] 采用电沉积法制备了不同组分的CuAg纳米线,通过添加剂3,5⁃二氨基⁃1,2,4⁃三唑(DAT)来调控催化剂形貌,多孔纳米CuAg线在-0.70 V(vs.RHE)电位下,对C2+ 产物表现出较高的选择性,法拉第效率为85.0%.S.Ma等[33 ] 通过改变不同Cu、Pd原子配比及排列方式,制备出3种不同Cu⁃Pd合金催化剂,还原产物C2 H4 的选择性较高,相分离Cu⁃Pd催化剂法拉第效率可达48.0%.T.T.Zhuang等[34 ] 合成了缺陷可控的新型核⁃壳⁃空位铜(Cu2 S⁃Cu⁃V)纳米催化剂,通过催化剂核中掺杂硫原子并在壳层中引入铜空位,显著增强了多碳醇产物的选择性.Z.Y.Chang等[35 ] 采用一步还原法制备了不同Ag核、Cu修饰Ag核、Ag@Cu⁃20核壳结构纳米粒子催化剂,产物逐渐显示出由CO到碳氢化合物的变化,还原产物C2 H4 的法拉第效率为28.6%.D.Ren等[36 ] 制备了氧化物衍生的铜锌催化剂用于还原成乙醇,通过锌的质量控制乙醇的选择性,在-1.05 V(vs. RHE)条件下,Cu4 Zn对乙醇的选择性最好,达到29.1%,并5 h内保持稳定. ...
1
... T.T.H.Hoang等[32 ] 采用电沉积法制备了不同组分的CuAg纳米线,通过添加剂3,5⁃二氨基⁃1,2,4⁃三唑(DAT)来调控催化剂形貌,多孔纳米CuAg线在-0.70 V(vs.RHE)电位下,对C2+ 产物表现出较高的选择性,法拉第效率为85.0%.S.Ma等[33 ] 通过改变不同Cu、Pd原子配比及排列方式,制备出3种不同Cu⁃Pd合金催化剂,还原产物C2 H4 的选择性较高,相分离Cu⁃Pd催化剂法拉第效率可达48.0%.T.T.Zhuang等[34 ] 合成了缺陷可控的新型核⁃壳⁃空位铜(Cu2 S⁃Cu⁃V)纳米催化剂,通过催化剂核中掺杂硫原子并在壳层中引入铜空位,显著增强了多碳醇产物的选择性.Z.Y.Chang等[35 ] 采用一步还原法制备了不同Ag核、Cu修饰Ag核、Ag@Cu⁃20核壳结构纳米粒子催化剂,产物逐渐显示出由CO到碳氢化合物的变化,还原产物C2 H4 的法拉第效率为28.6%.D.Ren等[36 ] 制备了氧化物衍生的铜锌催化剂用于还原成乙醇,通过锌的质量控制乙醇的选择性,在-1.05 V(vs. RHE)条件下,Cu4 Zn对乙醇的选择性最好,达到29.1%,并5 h内保持稳定. ...
2
... 多金属铜基催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/V电解液 法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH CRD⁃Cu3 Pd -1.20 0.1 mol/L KHCO3 40.6 [31 ] FL⁃Pd3 Cu -0.90 0.1 mol/L KHCO3 82.1 [31 ] CuAg 纳米线 -0.70 1.0 mol/L KOH 60.0 25.0 85.0 [32 ] 相分离CuPd -0.74 1.0 mol/L KOH 48.0 15.0 63.0 [33 ] Ag@Cu⁃20 -1.06 0.1 mol/L KHCO3 28.6 [35 ] 氧化物衍生Cu4 Zn层 -1.05 0.1 mol/L KHCO3 0.4 10.8 29.1 10.4 0.3 [36 ] Cu@CuPd纳米线 -0.30 0.5 mol/L KHCO3 80.0 [39 ] Cu@CuPd纳米线 -0.80 0.5 mol/L KHCO3 86.0 [39 ] Cu2 O/CuO@Ni -1.20 0.5 mol/L KHCO3 95.0 [40 ] Pd85 Cu15 /C -0.89 0.1 mol/L KHCO3 86.0 [41 ] Cu/Co纳米线 -0.65 0.1 mol/L KHCO3 80.0 [42 ]
2.2.1 碳氢化合物 W.J.Zhu等[31 ] 制备的凹菱形十二面体Cu3 Pd(CRD⁃Cu3 Pd)催化剂催化ERC反应的初始电位较纯Cu箔降低了200 mV,在-1.20 V(vs. RHE)电位下,生成CH4 的法拉第效率最高为40.6%,是纯Cu箔的2倍,其高选择性源于低配位指数和组成效应的协同作用. ...
... T.T.H.Hoang等[32 ] 采用电沉积法制备了不同组分的CuAg纳米线,通过添加剂3,5⁃二氨基⁃1,2,4⁃三唑(DAT)来调控催化剂形貌,多孔纳米CuAg线在-0.70 V(vs.RHE)电位下,对C2+ 产物表现出较高的选择性,法拉第效率为85.0%.S.Ma等[33 ] 通过改变不同Cu、Pd原子配比及排列方式,制备出3种不同Cu⁃Pd合金催化剂,还原产物C2 H4 的选择性较高,相分离Cu⁃Pd催化剂法拉第效率可达48.0%.T.T.Zhuang等[34 ] 合成了缺陷可控的新型核⁃壳⁃空位铜(Cu2 S⁃Cu⁃V)纳米催化剂,通过催化剂核中掺杂硫原子并在壳层中引入铜空位,显著增强了多碳醇产物的选择性.Z.Y.Chang等[35 ] 采用一步还原法制备了不同Ag核、Cu修饰Ag核、Ag@Cu⁃20核壳结构纳米粒子催化剂,产物逐渐显示出由CO到碳氢化合物的变化,还原产物C2 H4 的法拉第效率为28.6%.D.Ren等[36 ] 制备了氧化物衍生的铜锌催化剂用于还原成乙醇,通过锌的质量控制乙醇的选择性,在-1.05 V(vs. RHE)条件下,Cu4 Zn对乙醇的选择性最好,达到29.1%,并5 h内保持稳定. ...
2
... 多金属铜基催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/V电解液 法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH CRD⁃Cu3 Pd -1.20 0.1 mol/L KHCO3 40.6 [31 ] FL⁃Pd3 Cu -0.90 0.1 mol/L KHCO3 82.1 [31 ] CuAg 纳米线 -0.70 1.0 mol/L KOH 60.0 25.0 85.0 [32 ] 相分离CuPd -0.74 1.0 mol/L KOH 48.0 15.0 63.0 [33 ] Ag@Cu⁃20 -1.06 0.1 mol/L KHCO3 28.6 [35 ] 氧化物衍生Cu4 Zn层 -1.05 0.1 mol/L KHCO3 0.4 10.8 29.1 10.4 0.3 [36 ] Cu@CuPd纳米线 -0.30 0.5 mol/L KHCO3 80.0 [39 ] Cu@CuPd纳米线 -0.80 0.5 mol/L KHCO3 86.0 [39 ] Cu2 O/CuO@Ni -1.20 0.5 mol/L KHCO3 95.0 [40 ] Pd85 Cu15 /C -0.89 0.1 mol/L KHCO3 86.0 [41 ] Cu/Co纳米线 -0.65 0.1 mol/L KHCO3 80.0 [42 ]
2.2.1 碳氢化合物 W.J.Zhu等[31 ] 制备的凹菱形十二面体Cu3 Pd(CRD⁃Cu3 Pd)催化剂催化ERC反应的初始电位较纯Cu箔降低了200 mV,在-1.20 V(vs. RHE)电位下,生成CH4 的法拉第效率最高为40.6%,是纯Cu箔的2倍,其高选择性源于低配位指数和组成效应的协同作用. ...
... T.T.H.Hoang等[32 ] 采用电沉积法制备了不同组分的CuAg纳米线,通过添加剂3,5⁃二氨基⁃1,2,4⁃三唑(DAT)来调控催化剂形貌,多孔纳米CuAg线在-0.70 V(vs.RHE)电位下,对C2+ 产物表现出较高的选择性,法拉第效率为85.0%.S.Ma等[33 ] 通过改变不同Cu、Pd原子配比及排列方式,制备出3种不同Cu⁃Pd合金催化剂,还原产物C2 H4 的选择性较高,相分离Cu⁃Pd催化剂法拉第效率可达48.0%.T.T.Zhuang等[34 ] 合成了缺陷可控的新型核⁃壳⁃空位铜(Cu2 S⁃Cu⁃V)纳米催化剂,通过催化剂核中掺杂硫原子并在壳层中引入铜空位,显著增强了多碳醇产物的选择性.Z.Y.Chang等[35 ] 采用一步还原法制备了不同Ag核、Cu修饰Ag核、Ag@Cu⁃20核壳结构纳米粒子催化剂,产物逐渐显示出由CO到碳氢化合物的变化,还原产物C2 H4 的法拉第效率为28.6%.D.Ren等[36 ] 制备了氧化物衍生的铜锌催化剂用于还原成乙醇,通过锌的质量控制乙醇的选择性,在-1.05 V(vs. RHE)条件下,Cu4 Zn对乙醇的选择性最好,达到29.1%,并5 h内保持稳定. ...
1
... 多金属Cu基催化剂也可以得到除了碳氢化合物之外的其他产物.S.Rasul等[12 ] 制备的Cu⁃In合金催化剂在0.1 mol/L KHCO3 电解液中高选择地生成CO,法拉第效率为80.0%.Q.Li等[37 ] 在Cu表面包覆一层薄薄的SnO2 氧化层(约0.8 nm)后,催化剂则对CO具有很高选择性(-0.70 V(vs. RHE),法拉第效率为93.0%).然而,当SnO2 氧化层的厚度增加到1.8 nm时,则对HCOOH的生成具有很高的活性和选择性.H.J.Hu等[38 ] 通过电化学与热处理结合的方式制备Cu⁃Sn核/壳纳米线阵列催化剂,在0.5 mol/L KHCO3 中总电流密度为-13.2~-19.3 mA/cm2 ,产物CO的法拉第效率基本保持在90.0%~91.4%.Y.H.Hou等[39 ] 制备出一种新型的Cu@CuPd纳米线催化剂,在0.5 mol/L KHCO3 电解液和-0.30 V(vs. RHE)电位下,HCOOH的法拉第效率可以达到80.0%,而在-0.80 V(vs. RHE)电位下,CO的法拉第效率长时间(20 h)不低于86.0%.H.Yang等[40 ] 采用煅烧和快速电偶置换法结合制备了异质结构纳米线(Cu2 O/CuO@M),Cu2 O/CuO@Ni纳米线具有较高的催化活性,在0.5 mol/L KHCO3 电解液和-1.20 V(vs. RHE)电位下,还原产物是CO的法拉第效率高达95.0%,Cu2 O/CuO纳米线与Ni纳米粒子的杂化不仅具有调节d带中心以提高本征活性的作用,还可以提高对COOH*中间体的吸附能力,抑制析氢反应,进一步提高电催化剂对CO的转化效率. ...
1
... 多金属Cu基催化剂也可以得到除了碳氢化合物之外的其他产物.S.Rasul等[12 ] 制备的Cu⁃In合金催化剂在0.1 mol/L KHCO3 电解液中高选择地生成CO,法拉第效率为80.0%.Q.Li等[37 ] 在Cu表面包覆一层薄薄的SnO2 氧化层(约0.8 nm)后,催化剂则对CO具有很高选择性(-0.70 V(vs. RHE),法拉第效率为93.0%).然而,当SnO2 氧化层的厚度增加到1.8 nm时,则对HCOOH的生成具有很高的活性和选择性.H.J.Hu等[38 ] 通过电化学与热处理结合的方式制备Cu⁃Sn核/壳纳米线阵列催化剂,在0.5 mol/L KHCO3 中总电流密度为-13.2~-19.3 mA/cm2 ,产物CO的法拉第效率基本保持在90.0%~91.4%.Y.H.Hou等[39 ] 制备出一种新型的Cu@CuPd纳米线催化剂,在0.5 mol/L KHCO3 电解液和-0.30 V(vs. RHE)电位下,HCOOH的法拉第效率可以达到80.0%,而在-0.80 V(vs. RHE)电位下,CO的法拉第效率长时间(20 h)不低于86.0%.H.Yang等[40 ] 采用煅烧和快速电偶置换法结合制备了异质结构纳米线(Cu2 O/CuO@M),Cu2 O/CuO@Ni纳米线具有较高的催化活性,在0.5 mol/L KHCO3 电解液和-1.20 V(vs. RHE)电位下,还原产物是CO的法拉第效率高达95.0%,Cu2 O/CuO纳米线与Ni纳米粒子的杂化不仅具有调节d带中心以提高本征活性的作用,还可以提高对COOH*中间体的吸附能力,抑制析氢反应,进一步提高电催化剂对CO的转化效率. ...
3
... 多金属铜基催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/V电解液 法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH CRD⁃Cu3 Pd -1.20 0.1 mol/L KHCO3 40.6 [31 ] FL⁃Pd3 Cu -0.90 0.1 mol/L KHCO3 82.1 [31 ] CuAg 纳米线 -0.70 1.0 mol/L KOH 60.0 25.0 85.0 [32 ] 相分离CuPd -0.74 1.0 mol/L KOH 48.0 15.0 63.0 [33 ] Ag@Cu⁃20 -1.06 0.1 mol/L KHCO3 28.6 [35 ] 氧化物衍生Cu4 Zn层 -1.05 0.1 mol/L KHCO3 0.4 10.8 29.1 10.4 0.3 [36 ] Cu@CuPd纳米线 -0.30 0.5 mol/L KHCO3 80.0 [39 ] Cu@CuPd纳米线 -0.80 0.5 mol/L KHCO3 86.0 [39 ] Cu2 O/CuO@Ni -1.20 0.5 mol/L KHCO3 95.0 [40 ] Pd85 Cu15 /C -0.89 0.1 mol/L KHCO3 86.0 [41 ] Cu/Co纳米线 -0.65 0.1 mol/L KHCO3 80.0 [42 ]
2.2.1 碳氢化合物 W.J.Zhu等[31 ] 制备的凹菱形十二面体Cu3 Pd(CRD⁃Cu3 Pd)催化剂催化ERC反应的初始电位较纯Cu箔降低了200 mV,在-1.20 V(vs. RHE)电位下,生成CH4 的法拉第效率最高为40.6%,是纯Cu箔的2倍,其高选择性源于低配位指数和组成效应的协同作用. ...
... [39 ]
Cu2 O/CuO@Ni -1.20 0.5 mol/L KHCO3 95.0 [40 ] Pd85 Cu15 /C -0.89 0.1 mol/L KHCO3 86.0 [41 ] Cu/Co纳米线 -0.65 0.1 mol/L KHCO3 80.0 [42 ]
2.2.1 碳氢化合物 W.J.Zhu等[31 ] 制备的凹菱形十二面体Cu3 Pd(CRD⁃Cu3 Pd)催化剂催化ERC反应的初始电位较纯Cu箔降低了200 mV,在-1.20 V(vs. RHE)电位下,生成CH4 的法拉第效率最高为40.6%,是纯Cu箔的2倍,其高选择性源于低配位指数和组成效应的协同作用. ...
... 多金属Cu基催化剂也可以得到除了碳氢化合物之外的其他产物.S.Rasul等[12 ] 制备的Cu⁃In合金催化剂在0.1 mol/L KHCO3 电解液中高选择地生成CO,法拉第效率为80.0%.Q.Li等[37 ] 在Cu表面包覆一层薄薄的SnO2 氧化层(约0.8 nm)后,催化剂则对CO具有很高选择性(-0.70 V(vs. RHE),法拉第效率为93.0%).然而,当SnO2 氧化层的厚度增加到1.8 nm时,则对HCOOH的生成具有很高的活性和选择性.H.J.Hu等[38 ] 通过电化学与热处理结合的方式制备Cu⁃Sn核/壳纳米线阵列催化剂,在0.5 mol/L KHCO3 中总电流密度为-13.2~-19.3 mA/cm2 ,产物CO的法拉第效率基本保持在90.0%~91.4%.Y.H.Hou等[39 ] 制备出一种新型的Cu@CuPd纳米线催化剂,在0.5 mol/L KHCO3 电解液和-0.30 V(vs. RHE)电位下,HCOOH的法拉第效率可以达到80.0%,而在-0.80 V(vs. RHE)电位下,CO的法拉第效率长时间(20 h)不低于86.0%.H.Yang等[40 ] 采用煅烧和快速电偶置换法结合制备了异质结构纳米线(Cu2 O/CuO@M),Cu2 O/CuO@Ni纳米线具有较高的催化活性,在0.5 mol/L KHCO3 电解液和-1.20 V(vs. RHE)电位下,还原产物是CO的法拉第效率高达95.0%,Cu2 O/CuO纳米线与Ni纳米粒子的杂化不仅具有调节d带中心以提高本征活性的作用,还可以提高对COOH*中间体的吸附能力,抑制析氢反应,进一步提高电催化剂对CO的转化效率. ...
2
... 多金属铜基催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/V电解液 法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH CRD⁃Cu3 Pd -1.20 0.1 mol/L KHCO3 40.6 [31 ] FL⁃Pd3 Cu -0.90 0.1 mol/L KHCO3 82.1 [31 ] CuAg 纳米线 -0.70 1.0 mol/L KOH 60.0 25.0 85.0 [32 ] 相分离CuPd -0.74 1.0 mol/L KOH 48.0 15.0 63.0 [33 ] Ag@Cu⁃20 -1.06 0.1 mol/L KHCO3 28.6 [35 ] 氧化物衍生Cu4 Zn层 -1.05 0.1 mol/L KHCO3 0.4 10.8 29.1 10.4 0.3 [36 ] Cu@CuPd纳米线 -0.30 0.5 mol/L KHCO3 80.0 [39 ] Cu@CuPd纳米线 -0.80 0.5 mol/L KHCO3 86.0 [39 ] Cu2 O/CuO@Ni -1.20 0.5 mol/L KHCO3 95.0 [40 ] Pd85 Cu15 /C -0.89 0.1 mol/L KHCO3 86.0 [41 ] Cu/Co纳米线 -0.65 0.1 mol/L KHCO3 80.0 [42 ]
2.2.1 碳氢化合物 W.J.Zhu等[31 ] 制备的凹菱形十二面体Cu3 Pd(CRD⁃Cu3 Pd)催化剂催化ERC反应的初始电位较纯Cu箔降低了200 mV,在-1.20 V(vs. RHE)电位下,生成CH4 的法拉第效率最高为40.6%,是纯Cu箔的2倍,其高选择性源于低配位指数和组成效应的协同作用. ...
... 多金属Cu基催化剂也可以得到除了碳氢化合物之外的其他产物.S.Rasul等[12 ] 制备的Cu⁃In合金催化剂在0.1 mol/L KHCO3 电解液中高选择地生成CO,法拉第效率为80.0%.Q.Li等[37 ] 在Cu表面包覆一层薄薄的SnO2 氧化层(约0.8 nm)后,催化剂则对CO具有很高选择性(-0.70 V(vs. RHE),法拉第效率为93.0%).然而,当SnO2 氧化层的厚度增加到1.8 nm时,则对HCOOH的生成具有很高的活性和选择性.H.J.Hu等[38 ] 通过电化学与热处理结合的方式制备Cu⁃Sn核/壳纳米线阵列催化剂,在0.5 mol/L KHCO3 中总电流密度为-13.2~-19.3 mA/cm2 ,产物CO的法拉第效率基本保持在90.0%~91.4%.Y.H.Hou等[39 ] 制备出一种新型的Cu@CuPd纳米线催化剂,在0.5 mol/L KHCO3 电解液和-0.30 V(vs. RHE)电位下,HCOOH的法拉第效率可以达到80.0%,而在-0.80 V(vs. RHE)电位下,CO的法拉第效率长时间(20 h)不低于86.0%.H.Yang等[40 ] 采用煅烧和快速电偶置换法结合制备了异质结构纳米线(Cu2 O/CuO@M),Cu2 O/CuO@Ni纳米线具有较高的催化活性,在0.5 mol/L KHCO3 电解液和-1.20 V(vs. RHE)电位下,还原产物是CO的法拉第效率高达95.0%,Cu2 O/CuO纳米线与Ni纳米粒子的杂化不仅具有调节d带中心以提高本征活性的作用,还可以提高对COOH*中间体的吸附能力,抑制析氢反应,进一步提高电催化剂对CO的转化效率. ...
1
... 多金属铜基催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/V电解液 法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH CRD⁃Cu3 Pd -1.20 0.1 mol/L KHCO3 40.6 [31 ] FL⁃Pd3 Cu -0.90 0.1 mol/L KHCO3 82.1 [31 ] CuAg 纳米线 -0.70 1.0 mol/L KOH 60.0 25.0 85.0 [32 ] 相分离CuPd -0.74 1.0 mol/L KOH 48.0 15.0 63.0 [33 ] Ag@Cu⁃20 -1.06 0.1 mol/L KHCO3 28.6 [35 ] 氧化物衍生Cu4 Zn层 -1.05 0.1 mol/L KHCO3 0.4 10.8 29.1 10.4 0.3 [36 ] Cu@CuPd纳米线 -0.30 0.5 mol/L KHCO3 80.0 [39 ] Cu@CuPd纳米线 -0.80 0.5 mol/L KHCO3 86.0 [39 ] Cu2 O/CuO@Ni -1.20 0.5 mol/L KHCO3 95.0 [40 ] Pd85 Cu15 /C -0.89 0.1 mol/L KHCO3 86.0 [41 ] Cu/Co纳米线 -0.65 0.1 mol/L KHCO3 80.0 [42 ]
2.2.1 碳氢化合物 W.J.Zhu等[31 ] 制备的凹菱形十二面体Cu3 Pd(CRD⁃Cu3 Pd)催化剂催化ERC反应的初始电位较纯Cu箔降低了200 mV,在-1.20 V(vs. RHE)电位下,生成CH4 的法拉第效率最高为40.6%,是纯Cu箔的2倍,其高选择性源于低配位指数和组成效应的协同作用. ...
1
... 多金属铜基催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/V电解液 法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH CRD⁃Cu3 Pd -1.20 0.1 mol/L KHCO3 40.6 [31 ] FL⁃Pd3 Cu -0.90 0.1 mol/L KHCO3 82.1 [31 ] CuAg 纳米线 -0.70 1.0 mol/L KOH 60.0 25.0 85.0 [32 ] 相分离CuPd -0.74 1.0 mol/L KOH 48.0 15.0 63.0 [33 ] Ag@Cu⁃20 -1.06 0.1 mol/L KHCO3 28.6 [35 ] 氧化物衍生Cu4 Zn层 -1.05 0.1 mol/L KHCO3 0.4 10.8 29.1 10.4 0.3 [36 ] Cu@CuPd纳米线 -0.30 0.5 mol/L KHCO3 80.0 [39 ] Cu@CuPd纳米线 -0.80 0.5 mol/L KHCO3 86.0 [39 ] Cu2 O/CuO@Ni -1.20 0.5 mol/L KHCO3 95.0 [40 ] Pd85 Cu15 /C -0.89 0.1 mol/L KHCO3 86.0 [41 ] Cu/Co纳米线 -0.65 0.1 mol/L KHCO3 80.0 [42 ]
2.2.1 碳氢化合物 W.J.Zhu等[31 ] 制备的凹菱形十二面体Cu3 Pd(CRD⁃Cu3 Pd)催化剂催化ERC反应的初始电位较纯Cu箔降低了200 mV,在-1.20 V(vs. RHE)电位下,生成CH4 的法拉第效率最高为40.6%,是纯Cu箔的2倍,其高选择性源于低配位指数和组成效应的协同作用. ...
1
... 与纯Cu催化剂相比,Cu的氧化态会影响ERC反应催化性能,基于氧化物衍生金属纳米结构的电催化剂可以实现低过电位下的CO2 还原[43 ] .铜氧化物及其衍生催化剂的CO2 还原产物比较结果见表3 . ...
1
... C.W.Li等[44 ] 通过氧化退火处理Cu基催化剂,而后进行电化学还原表面的氧化层,发现表面修饰后的Cu电极比未修饰的Cu电极对ERC反应更有效,这可能与适当厚度的Cu2 O层电催化还原引起的晶界结构有关.H.Mistry等[11 ] 证明了氧化物衍生Cu基催化剂表面粗糙度对CO2 的催化性能有影响,Cu氧化物的存在是降低催化起始电位和提高催化活性的关键. ...
2
... 铜氧化物及其衍生催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/Vc (KHCO3 )/(mol·L-1 )法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH CuOx -1.40 0.1 63.00 63.00 [45 ] 3.6 µm Cu2 O薄层 -0.99 0.1 0.32 34.26 16.37 50.78 0.43 3.94 [47 ] Cux -0.80 0.1 90.00 [48 ] Cu2 O衍生的Cu纳米颗粒 -1.10 0.1 4.00 33.00 2.50 22.50 [49 ]
C.W.Li等[44 ] 通过氧化退火处理Cu基催化剂,而后进行电化学还原表面的氧化层,发现表面修饰后的Cu电极比未修饰的Cu电极对ERC反应更有效,这可能与适当厚度的Cu2 O层电催化还原引起的晶界结构有关.H.Mistry等[11 ] 证明了氧化物衍生Cu基催化剂表面粗糙度对CO2 的催化性能有影响,Cu氧化物的存在是降低催化起始电位和提高催化活性的关键. ...
... Cu基催化剂的表面缺陷可以修饰和提高表面活性,因此被广泛用于电催化剂中.表面缺陷可以改变表面和次表面原子的配位环境,导致表面附近的电荷不平衡而增强电子的转移,进一步有效调节表面物种对催化剂的吸附[32 ] .郑耿锋课题组报道了一种含有氧空位的Cu基催化剂,在ERC反应中表现出较高的催化活性[45 ] .利用氧空位给CO2 提供大量的电子,有利于*CO、*COH中间产物的吸附及*CH2 的脱附,提高Cu基催化剂对C2 H4 的选择性,-1.40 V(vs. RHE)电位下,法拉第效率达到63.0%,且电流密度增大.氧空位的多少对C2 H4 产物有直接的影响,也会影响电流大小.韩布兴院士课题组通过原位电沉积Cu络合物的方法制备出三维树枝状Cu⁃Cu2 O复合材料[46 ] .在KCl为电解质溶液,-0.40 V(vs. RHE)电位下,过电位分别为0.53 V(CH3 COOH)和0.48 V(C2 H5 OH),C2+ 产物法拉第效率高达80.0%,电流密度为-11.5 mA/cm2 .其优异C2+ 产物选择性主要是由于电催化剂与Cu基底的接触电阻接近于0,同时在三维树突状结构中暴露出了丰富的活性位点,并具有合适的Cu(I)/Cu(0)活性位点比例. ...
1
... Cu基催化剂的表面缺陷可以修饰和提高表面活性,因此被广泛用于电催化剂中.表面缺陷可以改变表面和次表面原子的配位环境,导致表面附近的电荷不平衡而增强电子的转移,进一步有效调节表面物种对催化剂的吸附[32 ] .郑耿锋课题组报道了一种含有氧空位的Cu基催化剂,在ERC反应中表现出较高的催化活性[45 ] .利用氧空位给CO2 提供大量的电子,有利于*CO、*COH中间产物的吸附及*CH2 的脱附,提高Cu基催化剂对C2 H4 的选择性,-1.40 V(vs. RHE)电位下,法拉第效率达到63.0%,且电流密度增大.氧空位的多少对C2 H4 产物有直接的影响,也会影响电流大小.韩布兴院士课题组通过原位电沉积Cu络合物的方法制备出三维树枝状Cu⁃Cu2 O复合材料[46 ] .在KCl为电解质溶液,-0.40 V(vs. RHE)电位下,过电位分别为0.53 V(CH3 COOH)和0.48 V(C2 H5 OH),C2+ 产物法拉第效率高达80.0%,电流密度为-11.5 mA/cm2 .其优异C2+ 产物选择性主要是由于电催化剂与Cu基底的接触电阻接近于0,同时在三维树突状结构中暴露出了丰富的活性位点,并具有合适的Cu(I)/Cu(0)活性位点比例. ...
1
... 铜氧化物及其衍生催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/Vc (KHCO3 )/(mol·L-1 )法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH CuOx -1.40 0.1 63.00 63.00 [45 ] 3.6 µm Cu2 O薄层 -0.99 0.1 0.32 34.26 16.37 50.78 0.43 3.94 [47 ] Cux -0.80 0.1 90.00 [48 ] Cu2 O衍生的Cu纳米颗粒 -1.10 0.1 4.00 33.00 2.50 22.50 [49 ]
C.W.Li等[44 ] 通过氧化退火处理Cu基催化剂,而后进行电化学还原表面的氧化层,发现表面修饰后的Cu电极比未修饰的Cu电极对ERC反应更有效,这可能与适当厚度的Cu2 O层电催化还原引起的晶界结构有关.H.Mistry等[11 ] 证明了氧化物衍生Cu基催化剂表面粗糙度对CO2 的催化性能有影响,Cu氧化物的存在是降低催化起始电位和提高催化活性的关键. ...
1
... 铜氧化物及其衍生催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/Vc (KHCO3 )/(mol·L-1 )法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH CuOx -1.40 0.1 63.00 63.00 [45 ] 3.6 µm Cu2 O薄层 -0.99 0.1 0.32 34.26 16.37 50.78 0.43 3.94 [47 ] Cux -0.80 0.1 90.00 [48 ] Cu2 O衍生的Cu纳米颗粒 -1.10 0.1 4.00 33.00 2.50 22.50 [49 ]
C.W.Li等[44 ] 通过氧化退火处理Cu基催化剂,而后进行电化学还原表面的氧化层,发现表面修饰后的Cu电极比未修饰的Cu电极对ERC反应更有效,这可能与适当厚度的Cu2 O层电催化还原引起的晶界结构有关.H.Mistry等[11 ] 证明了氧化物衍生Cu基催化剂表面粗糙度对CO2 的催化性能有影响,Cu氧化物的存在是降低催化起始电位和提高催化活性的关键. ...
1
... 铜氧化物及其衍生催化剂的CO
2 还原产物比较结果
催化剂 E (vs. RHE)/Vc (KHCO3 )/(mol·L-1 )法拉第效率/% 文献 CH4 C2 H4 C2 H5 OH C2+ CO HCOOH CuOx -1.40 0.1 63.00 63.00 [45 ] 3.6 µm Cu2 O薄层 -0.99 0.1 0.32 34.26 16.37 50.78 0.43 3.94 [47 ] Cux -0.80 0.1 90.00 [48 ] Cu2 O衍生的Cu纳米颗粒 -1.10 0.1 4.00 33.00 2.50 22.50 [49 ]
C.W.Li等[44 ] 通过氧化退火处理Cu基催化剂,而后进行电化学还原表面的氧化层,发现表面修饰后的Cu电极比未修饰的Cu电极对ERC反应更有效,这可能与适当厚度的Cu2 O层电催化还原引起的晶界结构有关.H.Mistry等[11 ] 证明了氧化物衍生Cu基催化剂表面粗糙度对CO2 的催化性能有影响,Cu氧化物的存在是降低催化起始电位和提高催化活性的关键. ...
1
... 由于CO2 在水溶液中溶解度低,导致ERC反应传质极化较大,通过在Cu基催化剂表面添加还原电位接近于ERC电位的有机分子作为CO2 还原的助催化剂,形成铜⁃有机物复合催化剂,促进CO2 还原性能的同时抑制析氢反应(HER).近年来,研究人员对金属有机骨架材料(MOFs)的研究颇多,MOFs是由金属离子或团簇与有机配体协调组成的一种混合材料,其催化活性可通过灵活选择金属离子与有机配体来调控,并通过修饰官能团、调整形态使表面积增大[50 ] .Y.L.Qiu等[51 ] 将具有CO2 “捕获”功能的纳米尺度CuMOF加入沉积Cu基催化剂的气体扩散电极(GDE)中,利用MOF中不饱和金属与CO2 分子之间的配位作用,赋予GDE“捕获”CO2 的功能,并通过调控电极结构参数增加电极内部反应速度和微观环境压力,提高电极表面的CO2 浓度,缓解传质极化,将CH4 的法拉第效率提高了2~3倍,析氢副反应降低了30%.X.Y.Tan等[52 ] 在1,3,5⁃苯三羧酸(H3 BTC)配体存在的条件下,对Cu2 O逐步进行刻蚀、溶解、氧化为Cu2+ ,进一步与配体连接形成Cu⁃MOF,然后连接没有被溶解的Cu2 O,最终形成重构的Cu2 O@Cu⁃MOF催化剂,该催化剂的比表面积增加,对CO2 的吸附量也增加,是Cu2 O的10倍.在-1.70 V(vs. RHE)电位下,还原产物碳氢化合物的法拉第效率为79.4%,其CH4 的法拉第效率高达63.2%,CH4 与C2 H4 的法拉第效率比为3.89. ...
1
... 由于CO2 在水溶液中溶解度低,导致ERC反应传质极化较大,通过在Cu基催化剂表面添加还原电位接近于ERC电位的有机分子作为CO2 还原的助催化剂,形成铜⁃有机物复合催化剂,促进CO2 还原性能的同时抑制析氢反应(HER).近年来,研究人员对金属有机骨架材料(MOFs)的研究颇多,MOFs是由金属离子或团簇与有机配体协调组成的一种混合材料,其催化活性可通过灵活选择金属离子与有机配体来调控,并通过修饰官能团、调整形态使表面积增大[50 ] .Y.L.Qiu等[51 ] 将具有CO2 “捕获”功能的纳米尺度CuMOF加入沉积Cu基催化剂的气体扩散电极(GDE)中,利用MOF中不饱和金属与CO2 分子之间的配位作用,赋予GDE“捕获”CO2 的功能,并通过调控电极结构参数增加电极内部反应速度和微观环境压力,提高电极表面的CO2 浓度,缓解传质极化,将CH4 的法拉第效率提高了2~3倍,析氢副反应降低了30%.X.Y.Tan等[52 ] 在1,3,5⁃苯三羧酸(H3 BTC)配体存在的条件下,对Cu2 O逐步进行刻蚀、溶解、氧化为Cu2+ ,进一步与配体连接形成Cu⁃MOF,然后连接没有被溶解的Cu2 O,最终形成重构的Cu2 O@Cu⁃MOF催化剂,该催化剂的比表面积增加,对CO2 的吸附量也增加,是Cu2 O的10倍.在-1.70 V(vs. RHE)电位下,还原产物碳氢化合物的法拉第效率为79.4%,其CH4 的法拉第效率高达63.2%,CH4 与C2 H4 的法拉第效率比为3.89. ...
1
... 由于CO2 在水溶液中溶解度低,导致ERC反应传质极化较大,通过在Cu基催化剂表面添加还原电位接近于ERC电位的有机分子作为CO2 还原的助催化剂,形成铜⁃有机物复合催化剂,促进CO2 还原性能的同时抑制析氢反应(HER).近年来,研究人员对金属有机骨架材料(MOFs)的研究颇多,MOFs是由金属离子或团簇与有机配体协调组成的一种混合材料,其催化活性可通过灵活选择金属离子与有机配体来调控,并通过修饰官能团、调整形态使表面积增大[50 ] .Y.L.Qiu等[51 ] 将具有CO2 “捕获”功能的纳米尺度CuMOF加入沉积Cu基催化剂的气体扩散电极(GDE)中,利用MOF中不饱和金属与CO2 分子之间的配位作用,赋予GDE“捕获”CO2 的功能,并通过调控电极结构参数增加电极内部反应速度和微观环境压力,提高电极表面的CO2 浓度,缓解传质极化,将CH4 的法拉第效率提高了2~3倍,析氢副反应降低了30%.X.Y.Tan等[52 ] 在1,3,5⁃苯三羧酸(H3 BTC)配体存在的条件下,对Cu2 O逐步进行刻蚀、溶解、氧化为Cu2+ ,进一步与配体连接形成Cu⁃MOF,然后连接没有被溶解的Cu2 O,最终形成重构的Cu2 O@Cu⁃MOF催化剂,该催化剂的比表面积增加,对CO2 的吸附量也增加,是Cu2 O的10倍.在-1.70 V(vs. RHE)电位下,还原产物碳氢化合物的法拉第效率为79.4%,其CH4 的法拉第效率高达63.2%,CH4 与C2 H4 的法拉第效率比为3.89. ...
1
... Cu基催化剂的表面组成对ERC反应有重要影响.在Cu电极表面加入含氨基等官能团的有机物也可以有效调控Cu电极的性能.H.Mistry等[11 ] 对Cu电极表面进行氧等离子体改性,发现通过改性后的介孔泡沫Cu基催化剂对C2 烃类产物具有高的法拉第效率.M.S.Xie等[14 ] 通过氨基酸来修饰Cu纳米线,引入-NH3 + 2 和C3 等碳氢化合物.Y.L.Qiu等[53 ] 在Cu电极中添加含有-NH2 的甲酸甲酯(MC),利用MC中的-NH2 基团增加Cu电极表面活性位与ERC反应中间粒子(如COO*- 、CO*、CHO*等)结合强度,从而稳定中间粒子,增加对碳氢化合物的选择性,且降低电极表面的反应过电位,提高析氢过电位,抑制析氢副反应的发生.H.Liu等[54 ] 制备了一种新型的多巴胺包覆Cu纳米线(Cu NWs@PDA)催化剂,PDA上的氨基可以捕捉H+ ,使质子从电解质溶液中转移到催化界面,酚羟基可以调节Cu NWs与中间体CO*的稳定性,提升Cu NWs电极对CH4 的选择性和稳定性.Cu NWs和Cu NWs@PDA的还原产物CH4 的法拉第效率分别为13.0%和30.0%,Cu NWs@PDA在14 h内稳定性较好,有机物修饰后的Cu NWs提高了对CH4 的选择性. ...
1
... Cu基催化剂的表面组成对ERC反应有重要影响.在Cu电极表面加入含氨基等官能团的有机物也可以有效调控Cu电极的性能.H.Mistry等[11 ] 对Cu电极表面进行氧等离子体改性,发现通过改性后的介孔泡沫Cu基催化剂对C2 烃类产物具有高的法拉第效率.M.S.Xie等[14 ] 通过氨基酸来修饰Cu纳米线,引入-NH3 + 2 和C3 等碳氢化合物.Y.L.Qiu等[53 ] 在Cu电极中添加含有-NH2 的甲酸甲酯(MC),利用MC中的-NH2 基团增加Cu电极表面活性位与ERC反应中间粒子(如COO*- 、CO*、CHO*等)结合强度,从而稳定中间粒子,增加对碳氢化合物的选择性,且降低电极表面的反应过电位,提高析氢过电位,抑制析氢副反应的发生.H.Liu等[54 ] 制备了一种新型的多巴胺包覆Cu纳米线(Cu NWs@PDA)催化剂,PDA上的氨基可以捕捉H+ ,使质子从电解质溶液中转移到催化界面,酚羟基可以调节Cu NWs与中间体CO*的稳定性,提升Cu NWs电极对CH4 的选择性和稳定性.Cu NWs和Cu NWs@PDA的还原产物CH4 的法拉第效率分别为13.0%和30.0%,Cu NWs@PDA在14 h内稳定性较好,有机物修饰后的Cu NWs提高了对CH4 的选择性. ...